
中国科学院上海有机化学研究所-生物医药快讯-2025-07
2025年7月FDA批准4种新药,具体如下:

数据来源:Cortellis - Clarivate Analytics
结构式:
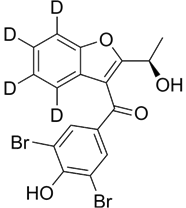
CAS No.:2173408-41-6
靶点/机制:SLC22A12蛋白抑制剂;
可能的适应症:痛风性关节炎; 高尿酸血症;原发性痛风
公司/组织:Arthrosi Therapeutics,广州瑞安博医药;
结构式:
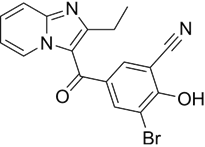
CAS No.:2088176-96-7
靶点/机制:SLC22A12尿酸转运蛋白抑制剂;
可能的适应症:痛风;
公司/组织:Atom Bioscience;
结构式:
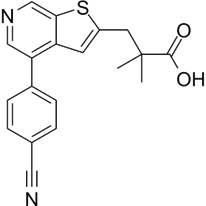
CAS No.:2013582-27-7
靶点/机制:尿酸盐转运蛋白 (URAT) 抑制剂;
可能的适应症:高尿酸血症;痛风;
公司/组织:上海璎黎药业;
结构式:
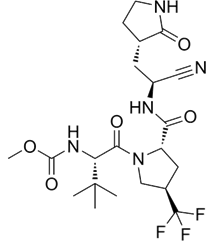
CAS No.:2755812-39-4
靶点/机制:SARS-CoV-2主要蛋白酶 (Mpro和3CLpro) 抑制剂;
可能的适应症:新冠病毒感染;
公司/组织:辉瑞;
结构式:
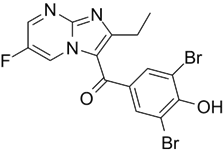
CAS No.:2365178-28-3
靶点/机制:尿酸盐转运子 (URAT) 抑制剂;
可能的适应症:痛风; 高尿酸血症;
公司/组织:苏州信诺维医药,Sinovent Pty;
结构式:
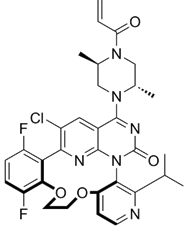
CAS No.:1661854-97-2
靶点/机制:KRAS G12C抑制剂;
可能的适应症:非小细胞肺癌;结直肠癌;
公司/组织:默沙东;
结构式:
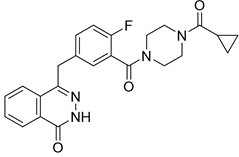
CAS No.:763113-22-0
靶点/机制:雄激素受体的PROTAC降解剂;
可能的适应症:非小细胞肺癌;结直肠癌;
公司/组织:礼来;
结构式:
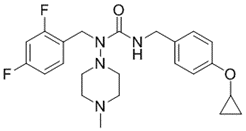
CAS No.:2289704-13-6
靶点/机制:磷酸鞘氨醇1受体激动剂;
可能的适应症:急性髓性白血病;
公司/组织:Kyorin Pharmaceutical,诺华;
结构式:
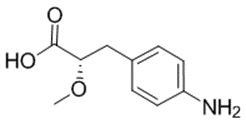
CAS No.:921195-93-9
靶点/机制:PPARγ激动剂;
可能的适应症:溃疡性结肠炎;
公司/组织:Giuliani;
结构式:
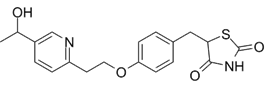
CAS No.:146062-44-4
靶点/机制:PPARγ激动剂;
可能的适应症:肾上腺脑发育不良症;
公司/组织:Minoryx Therapeutics,IDIBELL;
数据来源:Cortellis - Clarivate Analytics
结构式:
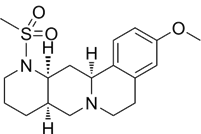
CAS No.:119905-05-4
靶点/机制:α2-肾上腺素受体拮抗剂;
可能的适应症:勃起功能障碍;
公司/组织:罗氏;
终止(discontinued)时间:1999/9;
终止原因:未知
结构式:
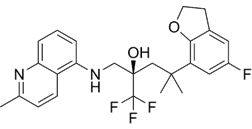
CAS No.:887375-26-0
靶点/机制:糖皮质激素受体激动剂;
可能的适应症:过敏性结膜炎;特应性皮炎;干眼症;
公司/组织:Bausch & Lomb,拜耳;
终止(discontinued)时间:2013/8;
终止原因:未知
结构式:
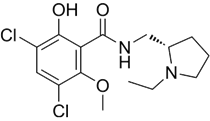
CAS No.:84225-95-6
靶点/机制:多巴胺D2/D3受体拮抗剂;
可能的适应症:注意力缺陷伴多动;
公司/组织:阿斯利康,耶鲁大学;
终止(discontinued)时间:2000;
终止原因:未知
结构式:
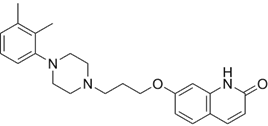
CAS No.:1329509-60-5
靶点/机制:突触前多巴胺受体激动剂和突触后 D2 受体的拮抗剂;
可能的适应症:精神障碍;
公司/组织:大冢制药;
终止(discontinued)时间:2001/1;
终止原因:未知
结构式:
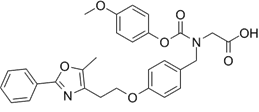
CAS No.:331741-94-7
靶点/机制:PPARα/γ双重激动剂;
可能的适应症:Ⅱ型糖尿病; 血脂障碍;
公司/组织:百时美施贵宝;
终止(discontinued)时间:2006/5;
终止原因:会导致水肿、心力衰竭、肾功能不全和体重增加
信息来源:Cortellis - Clarivate Analytics
结构式:
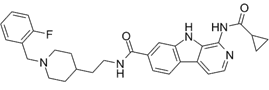
CAS No.:2765251-12-3
靶点/机制:乙酰胆碱酯酶抑制剂;
可能的适应症:阿尔兹海默症;
公司/组织:沈阳药科大学;
最早出现preclinical data时间:2022/2;
来源文献:Liu W et al., Eur J Med Chem, 2022, 229, 114095.
结构式:
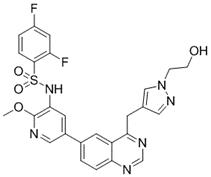
CAS No.:2269470-35-9
靶点/机制:PI3K抑制剂;
可能的适应症:肿瘤;
公司/组织:沈阳药科大学;
最早出现preclinical data时间:2020/6;
来源文献:Shu Wang et al, Cell Death & Disease, 2020, 11, 491.
结构式:
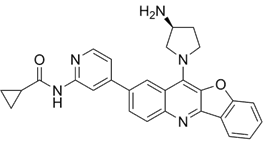
CAS No.:2851977-85-8
靶点/机制:CDK2和Topo I双重抑制剂;
可能的适应症:肿瘤;
公司/组织:沈阳药科大学;
最早出现preclinical data时间:2022/5;
来源文献:Huang Y et al., Bioorg Chem, 2022, 126, 105870.
结构式:
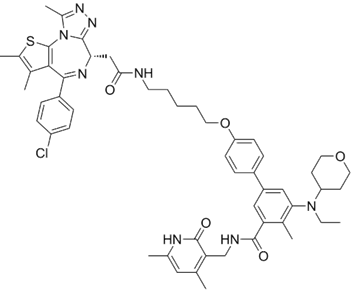
CAS No.:2770108-93-3
靶点/机制:EZH2和BRD4双重抑制剂;
可能的适应症:实体瘤;
公司/组织:中山大学;
最早出现preclinical data时间:2022/5;
来源文献:Guo Z et al., J Med Chem, 2022, 65(9), 6573-6592.
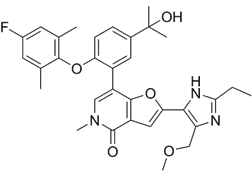
靶点/机制:BRD4抑制剂;
可能的适应症:白血病;
公司/组织:沈阳药科大学,中科院广州健康研究院;
最早出现preclinical data时间:2024/4;
来源文献:Tong JB et al., Mol Divers, 2024, 28(2), 671.
结构式:
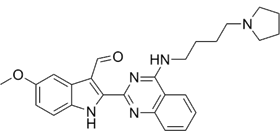
CAS No.:2415643-79-5
靶点/机制:ATPase调节剂;
可能的适应症:肥胖;
公司/组织:中山大学;
最早出现preclinical data时间:2020/4;
来源文献:Yong Rao et al., J Med Chem, 2020, 192, 112172.
结构式:
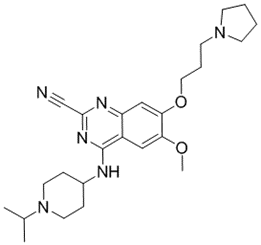
CAS No.:2761292-51-5
靶点/机制:赖氨酸甲基转移酶 G9a/NSD2 双重抑制剂;
可能的适应症:肿瘤;
公司/组织:中山大学;
最早出现preclinical data时间:2024/7;
来源文献:Chunju Yang et al., J Med Chem, 2024, 67(18), 16087.
结构式:
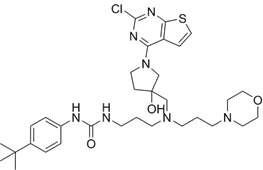
CAS No.:184582-62-5
靶点/机制:Disruptor of telomeric silencing 1-liked R231Q突变体抑制剂;
可能的适应症:肿瘤;
公司/组织:沈阳药科大学;
最早出现preclinical data时间:2024/9;
来源文献:Tan Z et al., J Med Chem, 2024, 67(18), 16248.
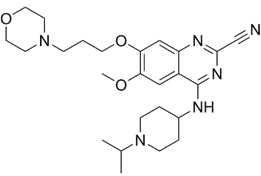
CAS No.:3051650-00-8
靶点/机制:NSD2抑制剂;
可能的适应症:肿瘤;
公司/组织:中山大学;
最早出现preclinical data时间:2024/9;
来源文献:Wei J et al., J Med Chem, 2024, 67(18), 16056.
结构式:
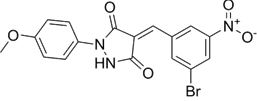
CAS No.:3035498-92-8
靶点/机制:ALKBH5共价抑制剂;
可能的适应症:三阴性乳腺癌;
公司/组织:中山大学;
最早出现preclinical data时间:2025/9;
来源文献:Yang X et al., J Med Chem, 2025, 68, 4133.
附件下载: